A Sinfonia da Vida: Água, pH e o Equilíbrio Perfeito
No vasto e intrincado universo da biologia, existe uma linguagem universal que dita cada batida do coração, cada pensamento e cada movimento: a bioquímica. Ela nos revela que a própria essência da vida, tal como a conhecemos, é uma dança delicada e harmoniosa de reações e processos moleculares. E no centro dessa coreografia vital, encontramos dois maestros insubstituíveis: a água e o pH. Para aqueles que se dedicam à área da saúde, desvendar os segredos químicos por trás desses conceitos não é apenas um exercício acadêmico, mas a chave mestra para compreender a complexidade da fisiologia humana e as nuances das patologias que afetam nossa existência.
A Água: O Berço Líquido da Vida
Imagine um mundo sem água. Impensável, não é? Em nosso próprio corpo, ela é a protagonista silenciosa, compondo cerca de 60% da nossa massa. Mas a água não é apenas um volume; é um solvente universal com propriedades mágicas, capaz de orquestrar a vida em seu nível mais fundamental. Sua estrutura dipolar, com um oxigênio ligeiramente negativo e hidrogênios ligeiramente positivos, confere-lhe uma capacidade ímpar de formar ligações de hidrogênio – elos invisíveis que, em sua vasta quantidade, moldam a viscosidade, a tensão superficial e a capacidade de absorver calor, características essenciais para a nossa sobrevivência. É a água que permite a dissipação do calor do cérebro para o sangue, mantendo nossa temperatura em um equilíbrio perfeito. E mais, ela é uma participante ativa em inúmeras reações metabólicas, um verdadeiro catalisador da vida.
O pH: O Termômetro da Acidez Vital
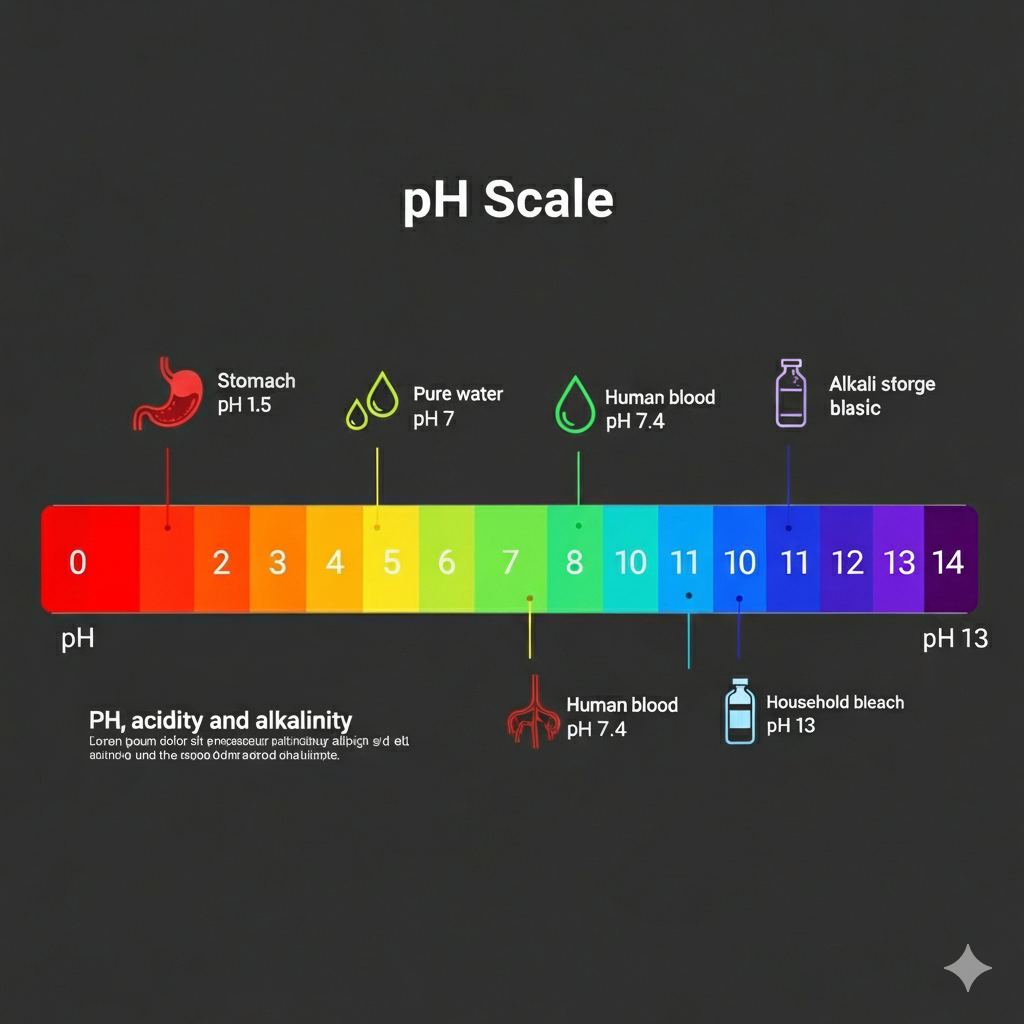
Manter um ambiente interno estável é a prioridade máxima do nosso corpo, um estado que chamamos de homeostase. E nesse cenário, o pH é um dos parâmetros mais rigorosamente controlados. Pense no pH do seu sangue arterial: ele se mantém em uma faixa incrivelmente estreita, entre 7,35 e 7,45. Uma pequena variação fora desses limites pode desencadear uma cascata de eventos com sérias consequências para a saúde. O pH é, em essência, a medida da concentração de íons hidrogênio – quanto mais íons, mais ácido; quanto menos, mais alcalino. A maioria das enzimas, as operárias incansáveis do nosso metabolismo, funciona otimamente em um pH entre 5 e 9. Qualquer desvio pode desativá-las, comprometendo vias metabólicas inteiras e, em última instância, a nossa saúde.
Sistemas Tampão: Os Guardiões do Equilíbrio
Para proteger nosso corpo das flutuações constantes de pH, resultantes da produção metabólica de ácidos e bases, a natureza nos dotou de sistemas de defesa extraordinários: os sistemas tampão. Pense neles como amortecedores químicos, misturas inteligentes de um ácido fraco e sua base conjugada, prontas para absorver ou liberar prótons e, assim, minimizar qualquer alteração brusca no pH. A eficácia de um tampão é máxima quando o pH está próximo do seu pKa, o ponto em que o ácido fraco está 50% dissociado.
Os principais guardiões desse equilíbrio em nosso corpo são:
1. Sistema Bicarbonato-Ácido Carbônico: Este é o campeão da regulação do pH no líquido extracelular, como o plasma sanguíneo. O dióxido de carbono (CO2), um subproduto natural do nosso metabolismo celular, encontra a água e, com a ajuda da enzima anidrase carbônica, se transforma em ácido carbônico. Este, por sua vez, se dissocia em íons hidrogênio e bicarbonato. A genialidade desse sistema reside na sua capacidade de ser regulado pelos pulmões (que controlam a eliminação de CO2 pela respiração) e pelos rins (que ajustam a excreção ou reabsorção de bicarbonato). É uma orquestra perfeita de órgãos trabalhando em harmonia para manter o pH ideal.
2. Sistema Tampão Fosfato: Embora menos abundante que o bicarbonato no plasma, o sistema tampão fosfato é um herói nos líquidos intracelulares. Com um pKa de 7,20, o fosfato inorgânico (H2PO4-/HPO42-) atua como um tampão eficaz, garantindo que o ambiente dentro de nossas células permaneça estável, protegendo as delicadas estruturas e processos que ali ocorrem.
3. Sistema Tampão de Proteínas: Nossas proteínas, incluindo a vital hemoglobina, são verdadeiros multitarefas. Além de suas inúmeras funções estruturais e catalíticas, elas são excelentes tampões. Graças aos seus grupos funcionais ionizáveis, como o grupo imidazol da histidina (com um pKa próximo ao pH fisiológico), as proteínas podem aceitar ou doar prótons, contribuindo significativamente para a manutenção do pH. A hemoglobina, em particular, desempenha um papel crucial no transporte de oxigênio para os tecidos e de CO2 e prótons de volta para os pulmões. Sua afinidade pelo oxigênio diminui quando o pH cai (o famoso efeito Bohr), garantindo que o oxigênio seja liberado exatamente onde é mais necessário: nos tecidos que estão produzindo mais CO2 e, consequentemente, se tornando mais ácidos.
Correlações Clínicas: Quando a Harmonia se Desfaz
Os desequilíbrios do pH, como a acidose (quando o pH sanguíneo cai abaixo de 7,35) e a alcalose (quando o pH sanguíneo sobe acima de 7,45), não são doenças em si, mas sim um grito de alerta do nosso corpo, indicando que algo mais profundo está acontecendo. São manifestações de um problema subjacente que precisa ser investigado.
Acidose Metabólica: O Alerta da Cetoacidose Diabética
Um exemplo dramático de como o equilíbrio do pH pode ser rompido é a cetoacidose diabética (CAD), uma complicação grave que afeta pacientes com diabetes mellitus tipo 1. Na ausência de insulina, o corpo, desesperado por energia, começa a quebrar gorduras de forma descontrolada. Esse processo gera subprodutos ácidos, os corpos cetônicos (como o ácido acetoacético e o ácido β-hidroxibutírico). Quando esses ácidos se acumulam, eles liberam íons H+, derrubando o pH do sangue. É como se o corpo estivesse sendo inundado por uma onda ácida. Em resposta a essa emergência, o organismo aciona mecanismos compensatórios, como a respiração de Kussmaul – uma respiração profunda e rápida que tenta eliminar o excesso de CO2 e, assim, elevar o pH sanguíneo, buscando desesperadamente restaurar a normalidade.
Alcalose Respiratória: A Armadilha da Hiperventilação
Por outro lado, a alcalose respiratória nos mostra como até mesmo um ato tão vital como a respiração pode, em excesso, desequilibrar o pH. Situações de ansiedade ou estresse podem levar à hiperventilação, onde eliminamos CO2 em demasia pelos pulmões. A queda abrupta na concentração de CO2 no sangue desvia o equilíbrio do sistema tampão bicarbonato, consumindo íons H+ e elevando o pH sanguíneo. É como se o corpo estivesse se tornando excessivamente alcalino. Em casos mais leves, isso pode se manifestar como tontura e formigamento, um lembrete sutil de que a harmonia interna foi perturbada.
Recursos Adicionais para Aprofundamento: Desvendando Mais Segredos
Para aqueles que desejam mergulhar ainda mais fundo nesse fascinante universo da bioquímica e da fisiologia, recomendamos os seguintes recursos:
•Sistemas-Tampão no Organismo Humano: Um artigo claro e conciso do blog SanarMed que explora a relevância dos sistemas tampão na homeostase. Acesse aqui.
•Regulação Ácido-Base: O MSD Manuals oferece uma visão detalhada dos distúrbios ácido-base, seus tipos e mecanismos compensatórios. Acesse aqui.
•Química da Água e pH: Para uma compreensão aprofundada das propriedades da água e da escala de pH, a Universidade Federal de Roraima (UFRR) disponibiliza um material didático online. Acesse aqui.
Esperamos que esta jornada pela química essencial da vida tenha sido tão esclarecedora quanto inspiradora. A compreensão desses fundamentos não apenas enriquece o conhecimento, mas também capacita os futuros profissionais de saúde a desvendar os mistérios do corpo humano e a promover o bem-estar de forma mais eficaz.
